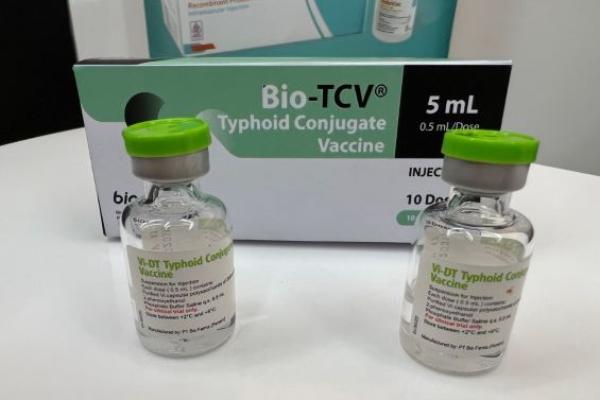
Vaksin Bio-TCV. Foto: dok. jurnas
JAKARTA, Jurnas.com - Badan Pengawas Obat dan Makanan (BPOM) sebagai otoritas pengawas obat dan makanan memberikan izin edar untuk vaksin konjugat tifoid (TCV) Bio-TCV milik Bio Farma di Indonesia.
“Dengan adanya bukti bahwa perubahan iklim dan meningkatnya resistensi antimikroba berdampak pada prevalensi dan tingkat keparahan demam tifoid, pencegahan penyakit melalui vaksinasi merupakan langkah kunci untuk pengendalian tifoid,” kata Wakil Direktur Jenderal, Klinis, Penilaian, Regulasi, Evaluasi Institut Vaksin Internasional (IVI), Dr. Sushant Sahasrabuddhe dalam keterangannya, Jumat (10/11/2023).
Bio-TCV adalah vaksin polisakarida Vi yang terkonjugasi dengan protein pembawa toksoid difteri (Vi-DT), yang awalnya dikembangkan di IVI dan dialihkan ke Bio Farma pada tahun 2014.
Peringatan Hari Pahlawan, Siti Fauziah: Implementasikan Nilai-Nilai Kepahlawanan Dalam Keseharian
Sejak awal, cakupan program pengembangan vaksin bersama ini meliputi pengembangan praklinis dan uji klinis Fase I-III yang diikuti dengan dukungan teknis melalui perizinan lokal dan pengajuan prakualifikasi (PQ) dari Organisasi Kesehatan Dunia (WHO).
Perizinan ini diperuntukkan bagi Perusahaan Aliansi Vaksin untuk membeli vaksin tersebut untuk digunakan dalam penggunaan kesehatan masyarakat secara global.
Kemitraan selama satu dekade dalam upaya mengembangkan TCV yang aman, efektif, dan terjangkau itu sebagian didanai oleh hibah dari Bill & Melinda Gates Foundation.
Direktur Utama Bio Farma Shadiq Akasya mengatakan izin edar tersebut merupakan bukti komitmen Bio Farma terhadap kesehatan global dalam memerangi penyakit menular melalui penyediaan vaksin yang aman.
“Bio TCV akan menjadi alat penting dalam pencegahan infeksi tifoid yang memberikan perlindungan terhadap penyakit ini sejak usia sembilan bulan,” ucap Shadiq.
IVI dan Bio Farma mengonfirmasi keamanan dan imunogenisitas dosis tunggal Vi-DT dan tidak kalah dengan kontrol TCV yang telah memenuhi syarat WHO dalam uji klinis fase III di tiga ibu kota provinsi di Indonesia.
Dengan hasil penelitian ini, BPOM menyetujui vaksin tersebut untuk digunakan secara nasional pada individu usia sembilan bulan hingga 45 tahun.
Bio Farma akan mengajukan dokumen untuk WHO PQ, yang jika tercapai akan menambah TCV dengan harga terjangkau ke pasar publik global yang akan tersedia untuk negara-negara berpenghasilan rendah melalui Global Alliance Vaccine Innitiative (GAVI).
Demam tifoid adalah penyakit demam yang berpotensi mengancam jiwa yang disebabkan oleh Salmonella typhi yang terutama menyerang anak-anak dan orang dewasa muda.
Menurut WHO, diperkirakan terdapat 11 hingga 20 juta kasus tifoid setiap tahunnya, sebagian besar terjadi di negara-negara berpenghasilan rendah dan menengah.
KEYWORD :Bio Farma BPOM Bio-TCV